一,我为什么对索马鲁肽情有独钟:
在目前上市的GLP-1药物中,我最看好的就是索马鲁肽,原因一是长效,二是可以口服,并且在降糖和减重相关的头对头试验中,战胜了礼来的长效GLP-1重磅药物度拉糖肽,称之为目前GLP-1药物中的最佳也不为过。而且诺和诺德再接再厉,在减肥上的适应症也已经获批,虽然目前全球市场竞争暂时落后于度拉糖肽(吃了上市晚的亏),但是凭借其优秀的性质,未来追赶甚至超越度拉糖肽成为GLP-1类最畅销的药物可能性是非常大的。
二,索马鲁肽后期的适应症之——阿尔兹海默症
偶然间看到一篇莫名其妙的消息——索马鲁肽开展治疗阿尔兹海默症,直接启动3700人的Ⅲa期临床试验。作为一个把药理知识全部还给老师了的混混,我表示完全看不懂,这其实颠覆了我的很多固有认知。首先,一个治疗糖尿病的药物,怎么会去治疗阿尔兹海默症呢?索马鲁肽作为GLP-1(高血糖素样肽)受体激动剂,可以刺激胰岛素分泌,降低高血糖素分泌,从现有的作用机理研究来看,还没有看到如何对阿尔兹海默症起作用。

不过一个客观事实是,目前人们对阿尔兹海默症的发病机理研究还不是很透彻,虽然有很多种假说,但是没有一种得到科学印证。现有的治疗药物仅能缓解症状,不能针对发病机理治愈阿尔兹海默症。而且国际上已经很久没有治疗阿尔兹海默症的新药获批上市了。另一个超越我思维认知的是绕过了Ⅱ期试验,直接进入大规模的Ⅲa临床试验。新药的临床试验分为Ⅰ-Ⅳ期:
第Ⅰ期是针对健康志愿者的评价药物安全性的试验。这里没有进行Ⅰ期试验很好理解,口服索马鲁肽已经在前期适应症中做过了Ⅰ期试验,证明了安全性。
Ⅱ期试验主要是针对患病人群的小规模的试验,用来评价药物的有效性和耐受性。Ⅱ期试验是对新药安全性和有效性的在评价,为将来大规模也是最烧钱的Ⅲ期临床试验确定治疗给药剂量方案提供依据。
所以在这里,直接跳过Ⅱ期试验,通过动物学模型和数据库中的真实世界分析直接进入Ⅲa试验会不会有一点冒险,有一点豪赌的感觉。成功了,索马鲁肽真有可能成为“药王”,但失败了,庞大的临床费用也就打水漂了。直接开展3700人这种大规模的临床试验,不知道为什么这么着急,或者是我的观念是过时的,太刻板了?不过由于GLP-1特殊的作用机理,其引起低血糖的风险非常小,在常规剂量下,基本无需担心因治疗阿尔兹海默症而引起低血糖。
三,索马鲁肽,芬特明-托吡酯,纳曲酮-安非他酮,奥利司他 哪个是性价比最高的减肥药?
2021年12月8日,四川大学某团队在国际顶级医学期刊Lancet 在线发表题为“Pharmacotherapy for adults with overweight and obesity: a systematic review and network meta-analysis of randomised controlled trials”的研究论文,这项系统评述和网络荟萃分析包括从 PubMed、Embase 和 Cochrane 图书馆 (CENTRAL) 搜索,用于超重和肥胖成人减肥药物的随机对照试验(截至2021 年 3 月 23 日)。搜索确定了14605次引用,其中143项符合条件的试验招募了49810名参与者。
数据分析:
除左卡尼汀外,与单独改变生活方式相比,所有药物都降低了体重。具体的减重数据请看下表:
| [OR] | [MD] | 效果 | |
| 左卡尼汀 | 0 | 0 | 无效 |
| 芬特明-托吡酯 | 8.02 | -7.97 | 有效 |
| GLP-1 受体激动剂 | 6.33 | -5.76 | 有效 |
| 索马鲁肽 | 9.82 | -11.41 | 有效 |
| 纳曲酮-安非他酮 | 2.69 | 缺失 | 有效 |
| 奥利司他 | 1.72 | -1.45 | 有效 |
[OR]:体重减轻≥5的比值,[MD]:体重变化百分比
该研究发现在超重和肥胖的成年人中,芬特明-托吡酯和 GLP-1 受体激动剂被证明是最好的减肥药物;在 GLP-1 激动剂中索马鲁肽可能是最有效的。超重和肥胖是全球健康问题,并导致多种健康问题,包括 2 型糖尿病、心血管疾病、抑郁症和恶性肿瘤。生活方式的改变可能会改善生活质量和健康结果,但只有 61% 的超重和肥胖者完成了生活方式计划。
虽然减肥手术,包括 Roux-en-Y 胃绕道术,可以为体重指数 (BMI) 非常高的人提供长期的并发症保护,但许多人可能不愿意接受他们认为的大手术。除了改变生活方式和减肥手术外,药物疗法是减肥的重要替代疗法或辅助疗法。
2016 年美国临床内分泌学会指南评估了目前批准用于成人肥胖慢性管理的五种药物(orlistat(奥利斯他), lorcaserin(绿卡色林), naltrexone–bupropion(纳曲酮), liraglutide(利拉鲁肽)及phentermine–topiramate(芬特明-托吡酯)。然而,2020 年,美国食品和药物管理局因癌症风险增加而要求停用lorcaserin(绿卡色林)。
2021 年,发表了四项关于索马鲁肽(一种新型GLP-1 受体激动剂)的试验,其结果似乎改变了实践。此外,存在关于使用其他抗糖尿病药物(包括 SGLT2 抑制剂、二甲双胍和pramlintide)治疗肥胖症的证据。该研究进行了系统评价和网络荟萃分析以评估药物的减肥效果和安全性,前提是除了改变生活方式外,还用于管理超重和肥胖成人的体重。
四,详细介绍一下索马鲁肽:
口服版的索马鲁肽是诺和诺德研发生产的,又叫司美格鲁肽,是一种胰高血糖素样肽1(GLP-1)受体激动剂,于2019年获得美国FDA批准上市。索马鲁肽对包括胰腺、心脏和肝脏等在内的多种重要器官具有有益作用。
1、索马鲁肽的结构和作用机制
索马鲁肽是一种胰高血糖素样肽-1受体激动剂,作为饮食和运动的辅助剂,用以促进2型糖尿病成年患者的血糖控制。其作用机制如下:
索马鲁肽是一种与人类GLP-1序列有着94%同源性的GLP-1类似物。它作为GLP-1受体激动剂,可与GLP-1受体结合并激活受体,通过刺激胰岛素分泌和降低胰高血糖素分泌来降低血糖。除此之外,索马鲁肽还可作用于消化道,延缓胃肠排空以增加饱腹感;可作用于大脑,抑制食欲;作用于心血管,修复受损内膜,改善内皮功能。
2.结构图如下(与人类GLP-1序列有着94%同源性):
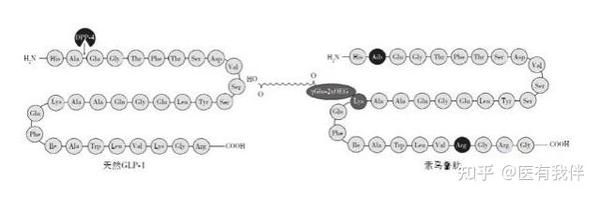
3,关于索马鲁肽的仿制版:
目前,索马鲁肽的口服版已经由诺和诺德公司历史15年研发出来了,这研发历程也只有诺和诺德这样的世界大药企才能承受的住啊。经过大批量的临床实验,瑞典批准了口服版索马鲁肽用于减肥的适应症(并命名为司美格鲁肽),并成功上市,原研版的请看下图:

话又说回来了,原研药耗费那么大的资金来研发,价格低不了吧。确实先不说有多贵,跟大家比喻一下,国内的工薪阶层一般都是接受不了的,也不排除有工薪阶层的领导土豪般的存在,想用原研的,那咱就管不着了。
在原研药上市之前,有很多粉丝就一直追问【医有我伴】,问有没有仿制药卖,原研的确实承担不起啊,我是深有感触,金钱对于一个人的重要性,也行对于穷人来说最好的消息就是仿制药已经出现了,因为自己的钱包可以不受委屈。诺和诺德授权日本MSD公司生产了仿制药,目前已经在多国上市,经过大批患者使用,效果和原研药基本相当,所以说到这里,仿制药在【医有我伴】心里面的地位就不言而喻了吧。对于【医有我伴】来说,团队要生存就要创造利润,但是我们也是有良知的,创造利润的同时能让患者少花钱,花对钱,有效果才是真正能体现我们价值的地方。又扯远了,请看下图司美格鲁肽仿制版:
4,口服版司美格鲁肽的使用方法:
a,开始服用索马鲁肽时,建议每次3mg,每天一次,持续30天。3mg索马鲁肽剂量用于开始疗法,对血糖控制是无效的。服用3mg剂量30天后,剂量增加,每次7mg(也可以3mg版两粒,因为司美是一盒100粒的,有时候药用不完别浪费了),每天一次。如果需要额外的血糖控制,服用7mg剂量至少30天后,剂量可以增加到每次14mg,每天一次。
不建议服用两片7mg的索马鲁肽来达到14 mg剂量。但是对于减肥患者来说,如果不是超重人士,7mg就足够了
b,和注射用司美格鲁肽的对比
针剂打0.25的,口服的用3mg
针剂打0.5的口服用7mg
针剂打1的口服用14mg.
c.服用索马鲁肽时应每日1次口服给药,需吞服整个片剂,避免切割,压碎或咀嚼药片。如果漏服一剂索马鲁肽,应跳过漏服剂量,第二天服用下一剂。因为每位患者的病情不同,在接受该药品治疗时用药剂量、疗程时间等也会有差异。患者是否可以一直使用索马鲁肽治疗主要是由自身情况决定的。患者在索马鲁肽治疗期间应严格按照医生的诊疗建议用药,不可擅自增加或减少用药剂量,避免因错误用药产生其他不良反应,耽误病情。
五,索马鲁肽注意事项和副作用是什么?
(1)使用限制:不建议使用RYBELSUS做为无法透过饮食及运动疗法有效控制血糖之第二型糖尿病病人第一线治疗。RYBELSUS未曾针对有胰脏炎病史的病人进行研究,有胰脏炎病史的病人,应考虑使用其他抗糖尿病疗法。不可用于治疗第一型糖尿病或糖尿病酮酸中毒,因为RYBELSUS对于此等情况无效。
(2)可追溯性:为提高生物制剂的追溯性,应清楚记录投与药品的名称及批号。
(3)全身性:Semaglutide不应使用于第一型糖尿病病人或治疗糖尿病酮酸中毒。胰岛素依赖型病人在开始接受 GLP-1 受体促效剂治疗时,若快速停用胰岛素或降低剂量,曾有糖尿病酮酸中毒的报告(请参关42节)。临床上没有用于纽约心脏学会(NYHA)第IV级郁血性心脏衰竭病人的经验,因此不建议将semaglutide 用于这类病人。
(4)胃肠道作用:使用GLP-1受体促效剂可能引起胃肠道不良反应,进而造成脱水,罕见情况下可导致肾功能恶化。告知接受semaglutide治疗的病人,胃肠道副作用可能导致脱水的风险,并注意避免体液不足。
(5)急性胰脏炎:使用GIP-受体促效剂的病人曾发生急性胰脏炎,告知病人急性胰脏炎的典型症状。疑似发生胰脏炎时,停用semaglutide。如果确诊,不可重新开始使用semaglutide。针对具有胰脏炎病史的病人,使用时应特别谨慎。
(6)低血糖:Semaglutide与磺醯脲类药物或胰岛素并用时,可能增加病人发生低血糖的风险(请参阅第 4.8节)。开始 semaglutide治疗时,降低磺醯脲类药物或胰岛素的剂量,可降低低血糖发生的风险。
(7)甲状腺C细胞肿瘤风险:在小鼠和大鼠中,具临床意义的semaglutide终生暴露量提高了甲状腺C细胞肿瘤(腺瘤及恶性肿瘤)发生率,且肿瘤与剂量、治疗持续时间均有相关。由于尚未确立 semaglutide 诱发啮齿类的甲状腺 C 细胞肿瘤是否与人类亦有相关性,因此目前并不清楚 RYBELSUS 是否会在人体内造成甲状腺C细胞肿瘤,包括髓质甲状腺癌(MTC)。
另一种GLP-1 受体促效剂 liraglutide上市后曾有MTC病例报告;但是就人体施用的经验而言,这些案例并不足以确立或排除GLP-1 受体促效剂与MTC之间的因果关系。
RYBELSUS 禁止用于本身或家族有 MTC病史的病人,或罹患MEN2的病人。提醒病人,RYBELSUS治疗可能引发MTC,以及甲状腺肿瘤的症状(例如颈部肿块、吞咽困难、呼吸困难、声音持续沙哑)。
接受RYBELSUS治疗的病人,定期监测血清降钙素或甲状腺超音波检查,是否有助于早期发现MTC,目前尚无定论。由于血清降钙素的检测专一性低,且甲状腺疾病的背景发生率高,所以这类监测可能增加不必要处置的风险。血清降钙素显著升高可能是MTC的表征,MTC病人的血清降钙素浓度一般>50ng/L。如果病人的血清降钙素检查发现升高,应进一步评估,身体检查或颈部造影如果发现甲状腺结节,也应进一步评估。
(8)糖尿病视网膜病变:糖尿病视网膜病变病人接受胰岛素及皮下注射semaglutide治疗后,曾观察到糖尿病视网膜病变并发症的风险增加,口服semaglutide也无法排除此风险(请参阅第48节)。糖尿病视网膜病变病人,并用semaglutide时特别谨慎。依据临床准则密切监测这些病人,并予以治疗。快速改善血糖控制可能与糖尿病视网膜病变短暂恶化有关,但无法排除其他机转。长期血糖控制可降低糖尿病视网膜病变的风险。
在使用RYBELSUS的血糖控制试验合并分析中,病人在试验期间曾通报糖尿病视网膜病变相关的不良反应(RYBELSUS4.2%,对照药物3.8%)。
在使用semaglutide注射剂(包含第二类糖尿病和高心血管风险的病人)的2年心血管结果中,曾有糖尿病视网膜病变并发症(为4项判定评估指标之一)发生于接受semaglutide注射剂治疗的病人(3.0%),此外接受安慰剂之病人亦有发生(1.8%)。基准点即有糖尿病视网膜病变病史的病人,其糖尿病视网膜病变并发症的绝对风险(semaglutide8.2%,安慰剂5.2%)高于没有糖尿病视网膜病变病史的病人(semaglutide0.7%,安慰剂0.4%)。
血糖控制快速改善,可能与糖尿病视网膜病变暂时恶化有关。长期以semaglutide控制血糖,对于糖尿病视网膜病变并发症有何影响,未曾进行研究。有糖尿病视网膜病变病史的病人,应密切监测视网膜病变是否恶化。
(9)急性肾损伤:上市后报告显示,接受GLP-1受体促效剂(包括semaglutide)治疮的病人中,曾发生急性肾捐伤和慢性肾功能衰竭恶化,有时可能需要进行血液透析。部分上述事件发生于未患有已知潜在肾脏疾病的病人。在大多数的通报事件中,病人曾出现恶心、呕吐、腹泻或脱水等症状。针对出现严重胃肠道不良反应的病人,如需开始施用RYBELSUS或递增剂量,请监测病人的肾功能变化。
(10)治疗反应:建议遵守给药方案,以达到semaglutide的最佳效果。如果使用semaglutide的治疗反应低于预期,则治疗医师应了解semaglutide的吸收变异很大、吸收量可能很小(2-4%的病人不会有任何暴露量),且 semaglutide的绝对生体可用率低。
(11)钠含量:本品每颗锭剂的钠含量23mg,相当于 WHO 建成人每日最大摄入量2克钠的 1%。

评论0